国务院新闻办公室定于2020年4月14日(星期二)上午10时举行新闻发布会,海关总署新闻发言人、统计分析司司长李魁文介绍2020年一季度进出口情况,并答记者问。
李魁文:
“近期,我们对医疗物资出口实施了相应监管。大家知道,在新冠肺炎疫情防控的特殊时期,进一步强化监管,规范医疗物资出口秩序,对更好地发挥我国医疗物资在全球抗击疫情中的作用具有重要意义。海关坚决贯彻党中央、国务院决策部署,强化监管,优化服务,支持有资质、有信誉的企业有序出口,为医疗物资走出国门、支持国际社会共同抗击疫情营造良好的通关环境。
最近我们会同有关部门发布了相关公告。医用物资质量安全直接关系人的生命健康,中国海关始终高度重视,采取有力措施,加强出口医用物资的监管。比如,前期联合发布了第5号公告,最近刚发布了第53号公告,也是为了进一步推动医疗物资的有序出口。海关将对相关工作情况做进一步解读和发布,希望大家关注相关专题新闻发布。”
根据海关总署2020年第53号公告,自4月10日起,对“6307900010”等海关商品编号项下的11类医疗物资实施出口商品检验,共涉及19个HS编码。之前,对出口检测试剂已实施卫生检疫。
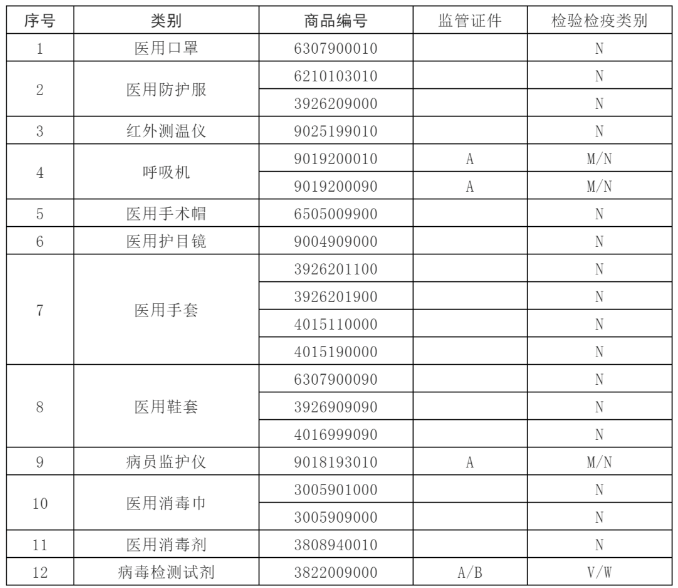
而海关总署第53号公告发出之后一天,4月11日海关就发布了一条紧急通知,针对53号公告做出了具体解释。再结合14号的新闻发布会中提到的公告解读。
无数人担心的“法检”,没有了。
一、出口申报
对53号公告所列11类出口法检医疗物资企业通过单一窗口申报报关,不同于其他出口法检商品的是,此次新增法检出口医疗物资无需实施产地检验,报关时无需出口电子底账。
(1)对出口法检医疗物资,企业需在报关单商品名称栏填报用途,并注明是否医用,检测试剂需注明是否为新型冠状病毒检测用。
温馨提示:同一HS编码下既有医疗物资又有非医疗物资的,应根据商品本身特征即生产制造标准,确定是否医用。
(2)对三部委“5号公告”所列(含公告后续调整所列)的出口新型冠状病毒检测试剂、医用口罩、医用防护服、呼吸机、红外体温计5类医疗物资,企业向海关报关时,须提供书面或电子声明和我国医疗器械产品注册证书。新冠病毒检测试剂还须提供药监部门出具的出口销售证明。
(3)对其他出口法检医疗物资,企业向海关报关时,应当提供医疗器械产品注册/备案证明和质量安全承诺声明。对无相关证明和承诺声明的,海关将实施严密监管。
(4)对新冠病毒检测试剂,发货人应当申请卫生检疫审批,凭《入/出境特殊物品卫生检疫审批单》通过单一窗口报检,经海关检验合格后,获得电子底账,报关时填写电子底账帐号。
郑重提示:企业必须按规定如实向海关申报,对将医用物资伪报为非医用物资的,依法从重处罚;涉嫌构成犯罪的,移送地方公安机关追究刑事责任。
二、质量安全要求
出口法检医疗物资应当符合进口国(地区)的要求,对进口国(地区)无质量安全标准要求的,应当符合我国质量安全标准。
海关总署关于印发
《海关实施出口医疗物资法定检验工作方案》的通知》
(署监发「2020」72号)
内容摘要及解读如下:
按照72号文件要求,对于53号公告规定的11类(19个商品编码)出口法检医疗物资,采取的是验证管理方式,就是不需要做商品品质检验,无需出口电子底账,企业正常申报报关单。
单证提交要求:在三部委发布的“5号公告”里的5类医疗物资,提交医疗器械产品注册证和企业承诺声明;在三部委发布的“5号公告”外的医用物资,企业提交注册证和质量安全承诺书,非医用物资不要求提交注册证和质量安全承诺书。
三、装运前检验
按照中国和国外政府签订的双边协议,对出口至部分国家和地区的商品需申请实施装运前检验。

声明: 企业是出口医疗物资质量安全第一责任人,海关依法实施检验监管。出口属于掺杂掺假、以假充真、以次充好的商品或者以不合格进出口商品冒充合格进出口商品的,将依法依规严厉查处;构成犯罪的,依法追究刑事责任。













